
Análise Crítica pela Direção em Laboratórios: Guia Completo conforme ISO 17025
A análise crítica pela direção é uma reunião formal e periódica em que a alta direção de uma organização ou laboratório avalia o desempenho do sistema de gestão da qualidade, revisa indicadores estratégicos e toma decisões sobre melhorias, recursos e mudanças necessárias. Para laboratórios de calibração e ensaio acreditados pela CGCRE/INMETRO, é um requisito obrigatório da norma ABNT NBR ISO/IEC 17025:2017.
Mais do que uma exigência burocrática, a análise crítica pela direção é uma ferramenta estratégica. É o momento em que os gestores reúnem todos os dados relevantes — auditorias, reclamações, não conformidades, indicadores, riscos — e tomam decisões que afetam o futuro do laboratório.
Em laboratórios bem geridos, a análise crítica pela direção não é vista como uma reunião formal de cumprimento de norma, mas como uma oportunidade real de avaliar resultados e definir prioridades para o próximo período.
Requisitos da ABNT NBR ISO/IEC 17025:2017
A norma ISO 17025, na seção 8.9, dedica um item específico à análise crítica pela direção. Os requisitos principais são:
- A direção deve analisar criticamente o sistema de gestão a intervalos planejados
- O objetivo é assegurar a contínua adequação, suficiência e eficácia do sistema
- Devem ser consideradas as políticas e objetivos declarados pelo laboratório
- Os registros da análise crítica devem ser mantidos
A norma é prescritiva quanto às entradas obrigatórias mas flexível quanto à frequência, formato e profundidade da análise. Cabe ao laboratório definir como conduzir o processo de forma adequada à sua realidade.
Entradas Obrigatórias da Análise Crítica
A norma ISO 17025 lista 15 entradas que devem ser consideradas na análise crítica pela direção. Vamos detalhar cada uma:
1. Mudanças em questões internas e externas
Avaliação de mudanças no contexto do laboratório: novos clientes, mudanças legais, novas tecnologias, alterações no quadro de pessoal, mudanças organizacionais.
2. Cumprimento dos objetivos
Análise dos indicadores estabelecidos pelo laboratório (ex: prazo médio de calibração, índice de satisfação do cliente, taxa de retrabalho) em relação às metas definidas.
3. Adequação das políticas e procedimentos
Verificação se as políticas da qualidade e os procedimentos operacionais continuam alinhados às necessidades do laboratório e dos clientes.
4. Status das ações de análises críticas anteriores
Acompanhamento das ações estabelecidas em reuniões anteriores: foram concluídas? Geraram os resultados esperados?
5. Resultados de auditorias internas
Análise das não conformidades, observações e oportunidades de melhoria identificadas em auditorias internas recentes.
6. Ações corretivas
Avaliação da eficácia das ações corretivas implementadas, incluindo análise de causa raiz e prevenção de recorrência.
7. Avaliações por organismos externos
Resultados de avaliações pela CGCRE/INMETRO, certificadoras ou outros organismos externos, incluindo não conformidades e prazos para tratamento.
8. Mudanças no volume e tipo de trabalho
Análise da evolução do volume de calibrações realizadas, novos tipos de serviço, mudanças no escopo de acreditação.
9. Retroalimentação de clientes e do pessoal
Feedback obtido por meio de pesquisas de satisfação, reuniões com clientes, reuniões com funcionários, sugestões internas.
10. Reclamações
Análise das reclamações recebidas, categorização por tipo, identificação de tendências e ações tomadas.
11. Eficácia de melhorias implementadas
Avaliação dos resultados alcançados pelas iniciativas de melhoria contínua executadas no período.
12. Adequação dos recursos
Verificação se o laboratório possui recursos suficientes — pessoal qualificado, equipamentos calibrados, instalações adequadas, infraestrutura tecnológica.
13. Resultados da identificação de riscos
Análise dos riscos identificados, avaliação de sua relevância e eficácia das ações de mitigação implementadas.
14. Resultados da garantia da validade dos resultados
Análise dos resultados de comparações interlaboratoriais, ensaios de proficiência, controle estatístico e demais atividades de garantia da qualidade.
15. Outros fatores relevantes
Atividades de monitoramento, treinamento, mudanças tecnológicas, oportunidades estratégicas e outros temas relevantes para a gestão.
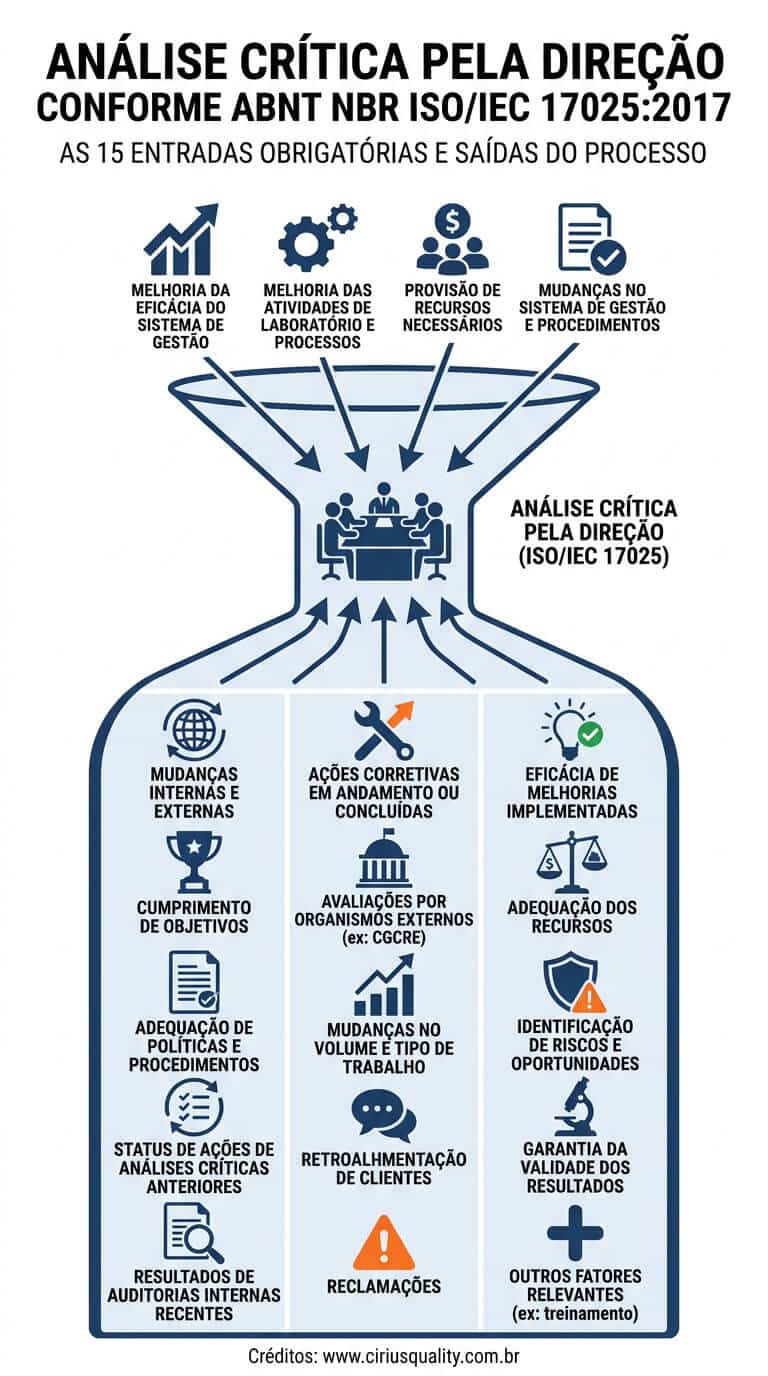
Saídas da Análise Crítica
A análise crítica pela direção deve gerar decisões e ações documentadas sobre:
- Melhoria da eficácia do sistema de gestão e seus processos
- Melhoria das atividades técnicas relacionadas ao cumprimento da norma
- Provisão de recursos necessários (financeiros, humanos, tecnológicos)
- Necessidade de mudanças no sistema de gestão, políticas ou objetivos
Frequência e Periodicidade
A norma não estabelece uma frequência específica, deixando essa decisão para o laboratório. Na prática, as opções mais comuns são:
- Anual: Frequência mais usual, adequada para laboratórios maduros e estáveis
- Semestral: Recomendada para laboratórios em fase de implantação, em processo de acreditação ou com sistema de gestão instável
- Trimestral: Em casos de reestruturação significativa ou após eventos críticos
- Extraordinária: Sempre que houver mudanças significativas como nova acreditação, mudança de escopo, fusão ou aquisição, ocorrências graves
A frequência escolhida deve ser documentada no procedimento de análise crítica e seguida sistematicamente.
Como Conduzir uma Análise Crítica Eficaz
Preparação
Antes da reunião, o coordenador da qualidade deve:
- Coletar dados de todas as 15 entradas obrigatórias
- Preparar relatórios consolidados com gráficos e indicadores
- Distribuir o material aos participantes com antecedência (mínimo 1 semana)
- Definir agenda da reunião com tempos por tópico
- Convocar os participantes (alta direção, gerentes, signatários autorizados)
Condução da Reunião
- Apresentar cada entrada com dados objetivos e indicadores
- Promover discussão crítica, não apenas apresentação de números
- Identificar tendências, padrões e correlações
- Avaliar a eficácia das ações anteriores
- Decidir sobre novas ações, recursos e mudanças
- Registrar todas as decisões com responsáveis e prazos
Documentação e Acompanhamento
Ao final da reunião, deve ser elaborada uma ata formal contendo:
- Data, local e participantes
- Entradas analisadas com resumo dos dados
- Discussões realizadas
- Decisões tomadas com justificativas
- Plano de ação com responsáveis e prazos
- Aprovação pela direção
A ata deve ser arquivada como registro permanente do sistema de gestão e disponibilizada para auditorias internas e externas.
Erros Comuns na Análise Crítica
- Tratar como reunião burocrática: Apenas cumprir o requisito sem realmente analisar criticamente os dados
- Não preparar dados antecipadamente: Reuniões sem preparação geram discussões superficiais
- Omitir entradas obrigatórias: Não considerar todas as 15 entradas requeridas pela norma
- Não definir ações concretas: Reunião sem decisões claras e acompanháveis
- Falta de acompanhamento: Não monitorar a execução das ações decididas
- Ausência da alta direção: Realizar a análise crítica sem a presença efetiva da direção
Perguntas Frequentes
Quem deve participar da análise crítica pela direção?
A alta direção do laboratório (diretor, gerente geral) é obrigatória. Recomenda-se também a participação do coordenador da qualidade, gerentes técnicos, signatários autorizados e responsáveis por áreas críticas. A composição depende do porte e estrutura do laboratório.
Posso fazer análise crítica por videoconferência?
Sim. A norma não exige presença física. O importante é que todos os participantes estejam presentes (mesmo que virtualmente), que a discussão seja efetiva e que a documentação seja adequada.
Quanto tempo deve durar uma análise crítica pela direção?
Não há tempo definido pela norma. Em laboratórios pequenos, 2 a 3 horas podem ser suficientes. Em laboratórios maiores ou com muitos dados a analisar, podem ser necessários um dia inteiro ou reuniões em múltiplas sessões. O importante é tempo suficiente para análise efetiva, não apenas apresentação.
Auditores podem solicitar a ata da análise crítica?
Sim. A ata é um registro do sistema de gestão e deve estar disponível para auditorias internas, da CGCRE/INMETRO e de outros organismos avaliadores. É um dos documentos mais solicitados em auditorias da ISO 17025.
Aprenda Mais com os Cursos Online da Cirius Quality
Para implementar uma análise crítica pela direção eficaz e em conformidade com a ISO 17025, conheça os cursos especializados:
- Curso Online Calibração de Equipamentos e Instrumentos de Medição — Domine os procedimentos completos de calibração e ajuste, desde o zero até o ajuste fino multipontos em transmissores inteligentes.
- Curso Online Análise de Certificado de Calibração — Aprenda a interpretar resultados de calibração e decidir quando o ajuste fino é necessário para atender aos critérios de aceitação.
- Curso Online de Metrologia — Fundamentos de metrologia, incerteza de medição e rastreabilidade para embasar suas decisões de ajuste e calibração.
- Curso Online MSA – Análises do Sistema de Medição – Este curso tem como objetivo descrever e ilustrar as principais funções e etapas do processo do MSA – Análises do Sistema de Medição, O MSA visa avaliação do sistema de medição e tem como objetivo principal identificar e corrigir falhas proveniente do processo de medição, cujo a finalidade é garantir a qualidade final dos produtos, além da melhoria contínua dos processos, produtos e serviços fornecidos pela organização e consequentemente atender as expectativas dos clientes.
Conclusão
A análise crítica pela direção é mais do que um requisito normativo — é uma ferramenta estratégica de gestão. Quando bem conduzida, ela transforma dados operacionais em decisões estratégicas, garantindo que o laboratório evolua continuamente e mantenha sua competência técnica e gerencial. Tratar essa atividade com a seriedade que merece é um diferencial competitivo importante.
Para aprofundar seus conhecimentos em análise crítica pela direção e gestão da qualidade laboratorial, conheça os cursos e serviços de consultoria da Cirius Quality. Com mais de 40 anos de experiência, ajudamos organizações a alcançar excelência em gestão da qualidade.










0 comments
Write a comment